1. LA BULLE
1.1 La forme sphérique
Il y a beaucoup d’éléments qui adoptent une forme géométrique stable. Une bulle de savon forme une sphère parfaite, lisse à l’échelle atomique et très peu déformable. Ainsi on comprend que la surface d’un liquide est donc comme une membrane tendue, caractérisée par une tension superficielle (ou tension de surface), qui s’oppose à ses déformations.
2.1.1 Définition de la tension superficielle
La tension superficielle ou énergie de surface, est la tension qui existe à la surface de séparation de deux milieux.
Quelques observations simples mettent en évidence ce phénomène :
· Un insecte capable de marcher sur l’eau
· Une pièce de monnaie flottant dans un verre
· Une bulle de savon
La tension superficielle dépend du liquide et de la nature de l’autre partie de l’interface (gaz, air, métal, verre, …).
2.1.2 Mécanisme de la tension superficielle
La tension superficielle g est la force appliquée perpendiculairement à la surface.
g=f/l
g en N.m-1 ou en J.m-2
f en N et l en m.
Dans un liquide les molécules sont soumises à plusieurs forces:
· Van der Waals (attraction)
· Électrostatiques (attraction ou répulsion)
Conséquence : Dans le cas d’une bulle de savon, qui est une mince couche de liquide emprisonnant une poche de gaz (air), celle-ci garde sa cohésion grâce à la tension superficielle. Tel qu’il existe une relation en pression intérieure et pression extérieure :
Pi – Pe = 4g/ R (1) équation de Laplace
Ou R est le rayon de la bulle.
De plus pour une bulle de savon, les tensioactifs contenus dans le film diminuent la tension superficielle, car ceux-ci dilatent la surface s’opposant à la tension de surface.
2.1.3 La forme sphérique
Comme nous l’avons vu, à l’intérieur d’un liquide les molécules s’attirent entre elles ; l’état d’équilibre est donc toujours celui où la surface de contact entre le liquide et l’air est la plus petite. C’est à dire la sphère car elle satisfait l’équation de Laplace (1).

Pour le liquide savonneux la forme stable est une goutte sphérique. Une bulle est un système hors d’équilibre donc instable : à la moindre petite fuite, elle se déchire et redevient une goutte.
C’est pour cela que les bulles ont une durée de vie aussi limitée et qu’elles éclatent aussi facilement à la moindre perturbation.
2.1 La durée de vie d’une bulle
Nous avons vu que la bulle prenait une forme sphérique pour répondre au théorème de Laplace. Qui plus est, l’équilibre de cette forme est vraiment très instable. Donc on peut se demander comment se maintient-elle quelques secondes voire quelques minutes en l’air pour finalement disparaitre ?

Schéma d’une paroi de bulle de savon
2.2.2 L’éclatement
On peut considérer qu’il existe trois facteurs pouvant provoquer l’éclatement :
· Le drainage.
La gravité entraine le liquide savonneux a s’écoulé entre les deux parois. Progressivement le film devient de plus en plus épais en bas alors qu’en haut il s’amincit, jusqu’à ce qu’il devienne trop fin et se rompt.
· L’humidité et la température.
Une bulle placée au soleil ou près d’une source de chaleur durera moins longtemps. En effet, la chaleur évapore l’eau de la paroi, et donc la fragilise.
A l’inverse un climat plutôt humide et froid favorisera la longévité de la bulle de savon.
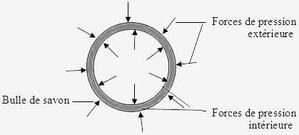
· Les forces de pression.
Les forces de pression à l'intérieur de la bulle ainsi que celles à l'extérieur sont une cause d'éclatement. En effet, une bulle renferme un certain volume de gaz, donc elle est constamment soumise aux forces de pression intérieure qui dilatent la bulle, l'étirent. Tandis que les forces de pression extérieures contractent la bulle pour la rendre plus petite.
Donc la bulle est soumise à des forces qui essayent de l'étirer et de la contracter simultanément : la bulle est en équilibre au niveau des forces.
En effet, la bulle s'étire jusqu'à ce que les pressions intérieures et extérieures à la bulle soient identiques. Cette dernière acquiert donc une certaine stabilité. Si en quelque endroit de la bulle, l'interface entre les deux couches d'air ne sont pas similaires (ex : écoulement de l’eau), les pressions appliquées au film n'influent pas de la même manière dessus : un point " moins épais " par exemple sera plus fragile. La bulle éclatera.
Remarque.
Plus le volume d’une bulle augmente plus celle-ci vie longtemps car le drainage de l’eau prendra plus de temps pour s’effectuer.

Durée de vie d’une bulle en fonction de son diamètre
En revanche pour de très gros volumes ce n’est pas le cas. Etant donné que la quantité de tensio-actif est fixée au départ, si on augmente la surface les tensio-actifs auront une densité plus faible que dans une petite bulle










 Schéma explicatif de la jauge Penning
Schéma explicatif de la jauge Penning Schéma explicatif du nanomètre de Piranni
Schéma explicatif du nanomètre de Piranni